
脑血管治疗
高度な再生医療が健康に役割を果たすようにしましょう
日期:2021-03-26 11:31作者:admin

这篇文章的概述
· Muse细胞最初存在于骨髓和皮肤(真皮)等体内,是能够分化为构成身体的各种细胞的干细胞
· 经监管机构批准,Muse细胞正在实施针对急性心肌梗死、脑梗死、大疱性表皮松解症及脊髓损伤患者的探索性临床试验
· Muse细胞有物质专利和分离专利两项专利
日本三菱化学子公司的生命科学研究所宣布,通过对皮肤疾病患者注射被称为“Muse细胞”的干细胞进行临床试验,确认了其安全性及效果(2020/7/29)。
这次临床试验的对象是5名皮肤有水泡等大疱性表皮松解症患者。
除了安全性之外,还验证了出现症状的皮肤面积是否缩小等效果,通过点滴给所有人注射了每人约1500万个Muse细胞。
之后观察52周,发现没有副作用等安全性问题,效果也得到了确认。
此次,对该Muse细胞进行概述。
目录
1.什么是Muse细胞
2.Muse细胞的特征
3.以急性心肌梗死患者为对象的临床试验
3-1.脑梗死的临床试验
3-2.脊髓损伤的临床试验
3-3.大疱性表皮松解症的临床试验
4.Muse细胞相关专利
1. 什么是Muse细胞
Muse细胞是在2010年由东北大学出泽真理教授等人的小组发现的细胞。干细胞最初存在于骨髓和皮肤(真皮)等体内,可以分化为构成身体的各种细胞。当Muse细胞被注入体内时,聚集在受损并修复组织。此外,由于是点滴注射,所以具有对身体的负担小、形成肿瘤的可能性低、一个Muse细胞制剂适用于多种疾病等优点(图1)。
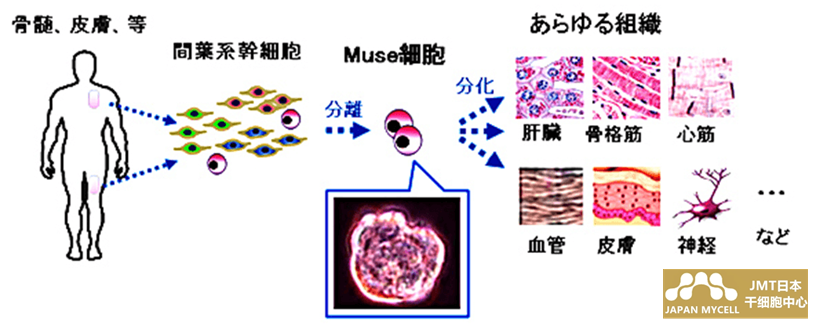
图1 Muse细胞的分离和活用影像
引用:国立研究开发法人新能源·产业技术综合开发机构
2. Muse细胞的特征
像人类一样的脊椎动物细胞的起源大致可分为三类。
1. 内胚层(成为消化道、肺、甲状腺、胰、肝、尿路等),
2. 间充质(成为骨髓、心肌、血管、血液、软骨、肌腱、脂肪组织),
3. 外肺叶(成为脑、脊髓、周围神经、表皮、毛发、指甲、乳腺、汗腺等)
Muse细胞是其中2的间充质干细胞,而且间充质干细胞既可以分化为内胚层,也可以分化为外肺叶。经过进一步的研究,发现了以下三个极好的性质:
· “很容易分离,很容易确保细胞数量”,也可以从他人移植。
· 有“高安全性”。不进行像胚胎来源干细胞和iPS细胞的基因导入一样的处理(有癌化的问题),从一开始就有多能性,所以几乎没有致瘤的危险
· 有“高疗效”。当Muse细胞被注入体内时,聚集在受损并修复组织。此外,因为是点滴注射,所以具有对身体的负担小、形成肿瘤的可能性低、一个Muse细胞制剂适用于多种疾病等优点
Muse细胞相关业务拓展是由日本生命科学研究所公司实施的。
该公司于2018年1月开始使用Muse细胞制剂(临床试验药名:CL2020)进行急性心肌梗死的探索性临床试验,确认其有效性和安全性,并经监管机构批准,正在实施针对急性心肌梗死、脑梗死、大疱性表皮松解症及脊髓损伤患者的探索性临床试验。
以下介绍来自生命科学研究所网站的信息。
3.以急性心肌梗死患者为对象的临床试验
本试验针对即使进行导管治疗,心功能也不能得到充分改善的急性心肌梗死患者,研究了在静脉内单次注射CL2020时的安全性、耐受性和有效性。
结果,关于主要评价项目CL2020注射后12周为止的安全性,没有发现特别的问题,此外,关于作为次要评价项目的有效性,作为心功能指标之一的左室射血分数有显著改善。
关于以Muse细胞产品(CL2020)的临床试验,即以急性心肌梗死患者为对象的探索性临床试验的论文,发表在一般社团法人日本循环器学会发行的学术杂志Circulation Journal的电子版上。
生命科学研究所认为,在此次试验中,CL2020显著改善了该患者的心功能,因此判断有可能为标准治疗不能取得充分效果的心肌梗死患者提供新的治疗方法,针对以急性心肌梗死患者为对象的CL2020,下一步验证性临床试验从2019年12月开始进行。

图2急性心肌梗死患者使用Muse细胞时的概略图
引用:生命科学研究所
3-1.脑梗死的临床试验
包括脑梗死在内的脑血管疾病(脑中风)是日本住院原因的第2位,并且是需要护理的原因的第1位(护理保险中需要护理的原因的不到20%)。
迄今为止,使用脑梗死模型进行的动物试验证实了静脉注射Muse细胞制剂可以改善运动功能障碍的效果。
考虑Muse细胞制剂可能通过修复受损的神经回路改善运动功能障碍,并成为治疗脑梗死的新选择。
[临床试验概要]
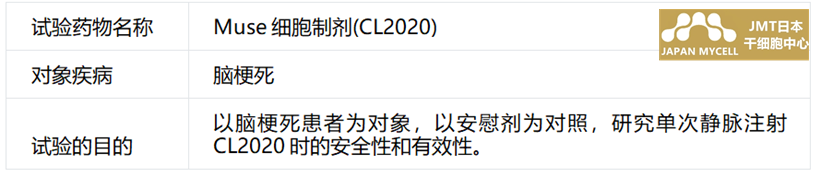
3-2.脊髓损伤的临床试验
针对脊髓损伤的临床试验将研究单次静脉注射对受伤2周左右的亚急性期患者的有效性和安全性。
临床试验中以16岁至75岁的脊髓损伤患者为对象,计划在筑波大学附属医院等10个设施实施。实施非盲,非对照试验。目标病例数为10例。之所以以亚急性期为对象,是因为急性期的炎症结束,血管生成·组织修复反应频繁发生的缘故。准备好后,开始给患者给药。
根据生命科学研究所,CL2020对脊髓损伤模型大鼠从急性期到亚急性期静脉注射1次或2次,结果发现后肢运动功能有改善的效果,可以步行。即使给药时间和给药次数不同,也发现了运动功能的改善效果,因此决定在临床上研究单次给药的有效性和安全性。
3-3. 大疱性表皮松解症的临床试验
北海道大学医院、东邦大学医疗中心大森医院等从2018年12月开始实施的以大疱性表皮松解症患者为对象的CL2020临床试验。
从本试验结果可以看出,CL2020给药后52周安全性没有特别的问题,有效性达到了最初的目标。
大疱性表皮松解症
大疱性表皮松解症是由于担负表皮~基底膜~真皮粘着的粘着结构分子天生少或消失,不能承受日常生活中施加在皮肤上的力,皮肤和粘膜摩擦而产生水泡和溃疡的疾病。已登记为国家指定疑难杂症,预计日本国内约有500-1000名患者,但现阶段没有有效的治疗方法,希望能开发出新的治疗方法。
4.Muse细胞相关专利
日本已获得包含以下两点的专利(第5185443号)。
1. 物质专利:可从活体间充质组织和培养间充质细胞中分离的两个细胞表面标记(SSEA-3和CD105)为阳性,不显示肿瘤性增殖,以及含有可自我复制的多能干细胞(Muse细胞)的细胞群体
2. 分离方法:从生物体的间充质组织和培养它们的间充质细胞中,以上述细胞表层标记为指标分离含有Muse细胞的细胞群的方法
也向欧美等国家申请了包括该内容及相关项目在内的专利,目前正在审查中。
关于本专利,发明者、申请人出泽教授等人授予了大学创业Clio株式会社独家使用权。之后,生命科学研究所于2017年1月1日吸收合并了全资子公司Clio株式会社,该公司解散。使用旧Clio株式会社的Muse细胞的再生医疗产品等的研究开发业务由生命科学研究所株式会社继承。

服务热线:400-161-8586
日本医疗观光株式会社运营日本:东京中央区日本橋大伝馬町10-1 柿原林業ビル2F
中国:江苏省苏州市工业园区广运国际金融中心408